Pacientă în vârstă de 65 de ani diagnosticată de 5 ani cu sclerodermie sistemică (SSc) forma cutanată difuză se prezintă pentru dispnee la eforturi mici, tuse seacă, astenie, fatigabilitate. Obiectiv: scor Rodnan modificat 31/50, raluri crepitante bazal bilateral („velcro-type”). Examinările de laborator: sindrom inflamator marcat, ANA (IF): 1/1280, cu topo I-like pattern; Anti-Scl-70 > 200 UR/ml. Capilaroscopie: tipar de “active scleroderma“. Pacienta prezenta scăderea marcată a DLCO (24% din valoarea prezisă); Probele funcționale respiratorii: FVC=61%; SaO2 în repaus=85%; Testul de mers 6 minute (6MWT): 300 m, SaO2 la 6MWT=77%; Scala Borg modificată=9. Diagnosticată cu hipertensiune pulmonară secundară într-un serviciu de cardiologie prin cateterism cardiac.
Tomografia computerizată de înaltă rezoluție (High Resolution Computer Tomography – HRCT) evidențiază modificări fibrotice avansate cu opacități reticulare, plaje de „sticlă mată” (mai puțin extensive decât patternul reticular) și bronșiectazii de tracțiune la nivelul ambilor câmpi pulmonari. Asociat există hipertransparențe chistice grupate, cu perete propriu (aspect în „fagure de miere”) situate subpleural, predominant la nivelul lobilor inferiori. Se remarcă și existența unor zone de cruțare a spațiului imediat subpleural („subpleural sparing” pattern) (Figura 1 A și B). Utilizând un protocol specific s-a calculat parenchimul pulmonar neafectat care reprezenta 41%.
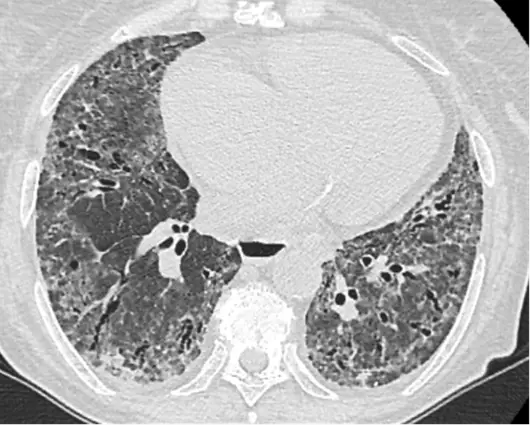
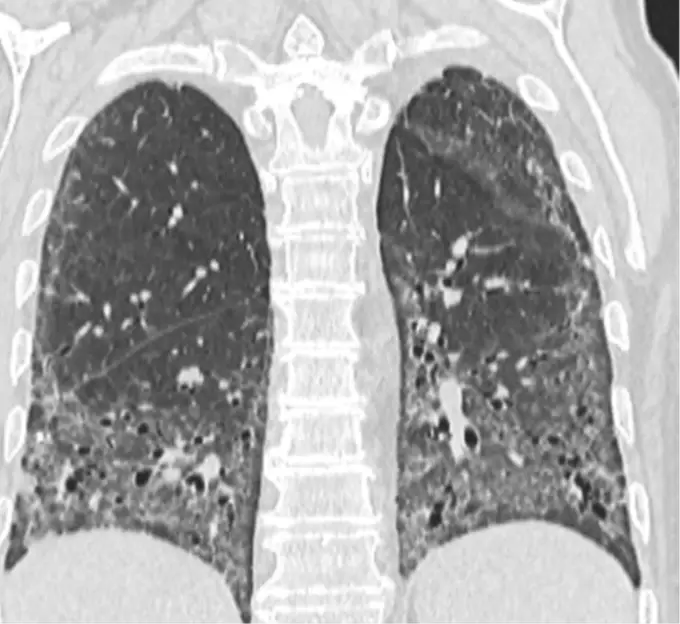
Figura 1. Tomografie computerizată de înaltă rezoluție (HRCT), secțiuni axiale (A) și coronale (B) evidențiază modificări fibrotice avansate cu opacități reticulare, plaje difuze de „sticlă mată” și bronșiectazii de tracțiune la nivelul ambilor câmpi pulmonari. Asociat există hipertransparențe chistice grupate, cu perete propriu (aspect în „fagure de miere”) situate subpleural, predominant la nivelul lobilor inferiori
Diagnostic final: Sclerodermie sistemică forma difuză. Pneumopatie interstițială fibrozantă progresivă. Hipertensiune pulmonară secundară.
A urmat tratament cu corticosteroizi și imunosupresoare în asociere cu tratamentul hipertensiunii pulmonare secundare, dar evoluția a fost nefavorabilă spre deces.
Pneumopatia interstițială difuză asociată sclerodermiei sistemice (PID-SSc) este o complicație frecventă, asociată cu morbiditate și mortalitate crescută. La toți pacienții nou diagnosticați cu SSc trebuie făcut screening pentru PID prin HRCT. Probele funcționale respiratorii și DLCO sunt instrumente adiționale pentru diagnosticul precoce.
HRCT este “standardul de aur” pentru diagnosticul non-invaziv al PID-SSc și pentru evaluarea severității bolii. Pe baza tipurilor de leziuni și topografiei lor au fost descrise mai multe pattern-uri imagistice caracteristice, care corespund tipurilor histologice de UIP (Usual Interstitial Pneumonia) și NSIP (Nonspecific Interstitial Pneumonia). La pacienții cu SSc afectarea pulmonară este mai frecvent de tip NSIP (~78%) și mai rar UIP (~7.5%).
Aspectul UIP la HRCT se caracterizează prin prezența de multiple leziuni microchistice cu perete propriu, grupate, situate în regiunile subpleurale și inferioare – aspect de „fagure de miere” („honeycombing”). La acestea se asociază bronșiectazii de tracțiune și opacități reticulare, fără leziuni/cu minime leziuni de „sticlă mată”. În cazul NSIP, cele mai frecvente leziuni sunt de „sticlă mată” („ground-glass opacities”) – opacități difuze care nu obstruează vascularizația subiacentă, cu distribuție predominant periferică și la nivelul lobilor inferiori. Un aspect considerat caracteristic este cruțarea spațiului imediat subpleural („subpleural sparing” pattern), aspect util pentru diferențierea NSIP de UIP. O parte din pacienți prezintă bronșiectazii de tracțiune și opacități reticulare, precum și leziuni microchistice subpleurale – aspecte imagistice întâlnite mai ales în tipul histologic de NSIP fibrotic. Coexistența pattern-urilor de NSIP și UIP este una din trăsăturile cheie care ajută la diferențierea UIP asociat colagenozelor de aspectul tipic de UIP din fibroza pulmonară idiopatică. Au fost descrise aspecte CT cu specificitate înaltă pentru UIP din colagenoze, care pot ajuta la diferențierea de UIP din fibroza pulmonară idiopatică: 1). predominanța fibrozei în segmentele anterioare ale lobilor superiori, concomitent cu afectarea lobilor inferiori și cruțarea celorlalte segmente ale lobilor superiori (“anterior upper lobe” sign); 2). formarea exuberantă de leziuni cu aspect de „fagure de miere” (“exuberant honeycombing” sign) și 3). distribuția izolată a fibrozei în lobii inferiori, astfel încât pe secțiunile coronale, interfața dintre zona de fibroză și plămânul normal poate fi aproximată cu o linie orizontală de-a lungul marginii superioare a zonei de fibroză (”straight edge” sign).
Scorurile de severitate și extensie a PID se bazează pe evaluarea următoarelor elemente CT: distribuția bolii, proporția modificărilor de reticulație și “sticlă mată” și extinderea fibrozei.
Progresia PID-SSc este heterogenă și trebuie monitorizată regulat. Evaluarea progresiei afectării pulmonare se face pe baza următorilor parametri: PFR (FVC și DLCO – valori absolute și reducerea față de baseline), extensia afectării interstițiale la HRCT, desaturarea indusă de efort și manifestările clinice. Factorii asociați cu riscul crescut de progresie a PID și mortalitate includ: a). factori demografici și clinici: vârsta mai înaintată, anticorpii anti-Scl-70, CRP crescut, scorul cutanat crescut, artrita; b). factori specifici PID: gradul dispneei, valoarea inițială scăzută a DLCO și FVC, desaturarea O2 în timpul 6MWT < 88%, extinderea fibrozei pe HRCT > 20%, extinderea aspectului de „fagure de miere” și prezența hipertensiunii pulmonare.
Deciziile terapeutice sunt determinate de severitatea/extensia PID-SSc și de riscul progresiei evaluate în mod regulat prin HRCT și PFR. Este importantă inițierea precoce a terapiei imunosupresoare și monitorizarea regulată a afectării interstițiale. Dacă progresia continuă sau răspunsul la tratament este neadecvat, se recomandă escaladarea terapiei.
Referințe:
- Ghid de diagnostic și tratament al pneumopatiilor interstițiale difuze 2015. Societatea Română de Pneumologie
- Capelli S, Bellando Randone S, Camiciottoli G, et al. Interstitial lung disease in systemic sclerosis: where do we stand? Eur Respir Rev. 2015;24:411-419
- Mueller-Mang C, Grosse C, Schmid K, et al. What Every Radiologist Should Know about Idiopathic Interstitial Pneumonias. RadioGraphics 2007; 27:595– 615
- Chung JH, Cox CW, Montner SM, et al. CT Features of the Usual Interstitial Pneumonia Pattern: Differentiating Connective Tissue Disease–Associated Interstitial Lung Disease from Idiopathic Pulmonary Fibrosis. Am J Roentgenol 2018; 210:307–13
- Hoffmann-Vold A-M, Allanore Y, Alves M, et al. Progressive interstitial lung disease in patients with systemic sclerosis-associated interstitial lung disease in the EUSTAR database. Ann Rheum Dis 2020;
